La desintegración radiactiva sería la piedra filosofal definitiva, la piedra que los alquimistas pensaban que podía convertir el plomo en oro o, de manera más general, un elemento químico en otro diferente.
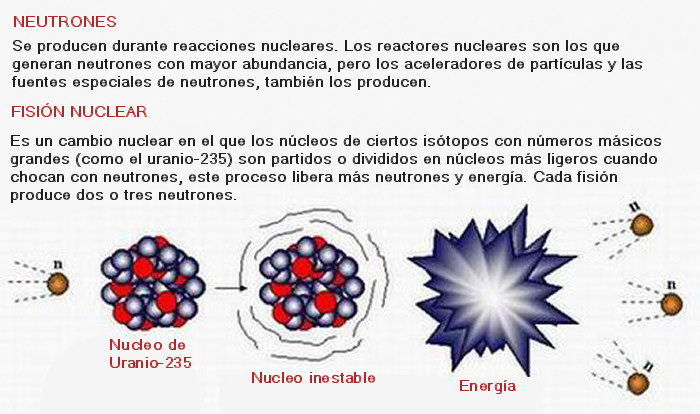
La energía implicada en la radiactividad proviene de la conversión de masa. Si medimos las masas de los productos finales de una desintegración radiactiva, encontraremos que poseen menos masa que el núcleo original.
El sobrante entre las masas de antes y después se convierte en energía según la ecuación E=mc2, y es esta energía la que podemos ver como la energía asociada con la radiación.
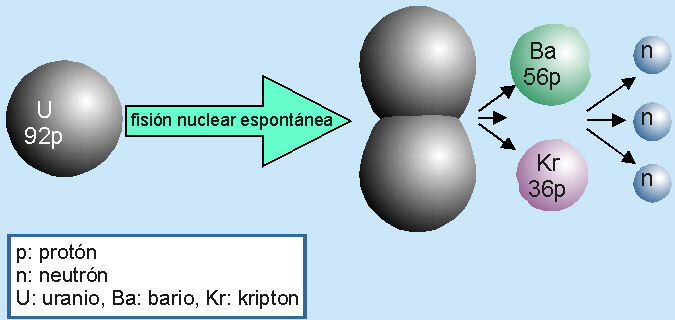
Debido a que la desintegración alfa y beta altera el número de protones en un núcleo, también transforma la identidad química del átomo del que ese núcleo forma parte.
Después de la desintegración alfa, un núcleo podrá incluir dos electrones menos de los que poseía antes de la desintegración. Los dos electrones “extra” terminarán distanciándose, dejando tras ellos un átomo que posee dos electrones menos en órbita.
Este átomo, por supuesto, será reconocido como un miembro de una especie química diferente del átomo original.

Una manera de pensar en la desintegración beta de un núcleo es pensar que uno de los neutrones dentro del núcleo padece una desintegración beta, creando un núcleo que tiene un protón más y un neutrón menos.
Siempre existen electrones libres a la deriva por ahí en la Naturaleza, y uno de ellos es absorbido finalmente por el átomo. El producto final es que aparece un nuevo elemento químico, uno con un electrón más en órbita de los que en principio había allí. De nuevo, un elemento químico nuevo ha sustituido al viejo.
Debido a que la desintegración gamma sólo conlleva una reorganización de protones y neutrones, no transforma un elemento en otro.

El uranio 238 se desintegra gracias a una emisión alfa. El uranio posee 92 protones en el núcleo, así que el núcleo hijo de esta desintegración tendrá 90 protones y una masa total de 234 (238 – 4). El resultado, de hecho, es lo que los químicos denominan torio 234 (234Th).
La desintegración de un núcleo apartado, raras veces es todo lo que ocurre en una desintegración radiactiva, debido a que la mayor parte de las veces los núcleos hijos (el producto de la desintegración) son también radiactivos.
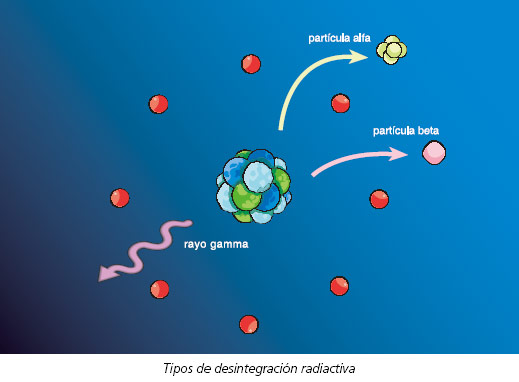
De esta manera, la desintegración original da lugar a un hijo que se desintegra, y ese núcleo se desintegra en otro, y así de manera sucesiva. Esta cadena de sucesos recibe el nombre de desintegración en cadena. La cadena continua hasta que se provoca un núcleo estable.
A raíz de la existencia de desintegraciones en cadena, una muestra pura de un elemento concreto se hallará pronto mezclada con otros elementos. Por ejemplo, el U-238 se desintegra en torio. El torio posteriormente se desintegra a través de emisiones beta en un elemento denominado protactinio, que a su vez se desintegra mediante emisión beta. Esta sucesión de desintegraciones sucesivas sigue adelante hasta que se llega al núcleo estable plomo 208.
La gente conoce los riesgos para la salud derivados de la acumulación de radón en las casas. El radón es uno de los elementos en la cadena de desintegraciones que conlleva del uranio al plomo. De esta menara, siempre se produce por las desintegraciones nucleares en el suelo. Una vez provocado un átomo de radón, su movimiento futuro se rige por su química que, en este caso, dictamina que no debe juntarse a materiales de su alrededor, sino que en vez de ello debe filtrarse al suelo y a los sótanos de las casas.

Los núcleos radiactivos no se descomponen juntos a la vez. Se desintegran en intervalos establecidos al azar. Contemplar esos núcleos desintegrarse es algo similar a observar el proceso de elaboración de palomitas de maíz, con los granos de maíz estallando en distintos intervalos.
La cifra que se emplea generalmente para medir la rapidez en que se descomponen los núcleos radiactivos, se denomina vida media. Esta medición determina el tiempo que requiere la mitad de los núcleos de un componente dado para llegar a descomponerse. De esta manera, si comenzamos con mil átomos, la vida media será el tiempo que deberemos esperar para que nos resten tan sólo quinientos.
Las vidas medias de los isótopos nucleares pueden clasificarse desde microsegundos hasta llegar a miles de millones de años. Estos son algunos ejemplos:
Carbono14 – 5.730±40 años.
Uranio 235 – 704 años.
Uranio 238 – 4.470 millones de años.
Uranio 239 – 23,5 minutos.
Cobalto 60 – 5.271 años.
Carbono 10 – 19,4 segundos.
Radón 222 – 3,82 días.
Yodo 131 – 8,02 días.
Radio 226 – 1.602 años.
Cesio 137 – 30,07 años.
Bismuto 207 – 31,55 años.
Estroncio 90 – 28,90 años.
Cadmio 109 – 462,6 días.
Oxígeno 15 – 122 segundos.