La química orgánica empezó como el estudio de las moléculas halladas en los sistemas vivos. Hubo un tiempo en que los químicos creían que las moléculas halladas en los sistemas vivos eran diferentes de aquellas halladas en los sistemas no vivos.
Cuando finalmente consiguieron sintetizar moléculas complejas en el siglo XIX, este punto de vista cambió, y se reconoció que las mismas leyes se aplicaban a la vez a la materia viva y a la no viva.
Hoy en día, el término “química orgánica” es usado generalmente para referirse al estudio de los compuestos que contienen carbono e hidrógeno, procedan de sistemas vivos o no. Así, alguien que intentara fabricar gasolina sintética sería considerado como un químico orgánico, aunque no empezara necesariamente con materiales tomados de sistemas vivos.
La química orgánica depende de los rasgos únicos del carbono, que tiene cuatro electrones en su órbita más externa. Esos electrones pueden unir el carbono, por medio del enlace covalente, a otros átomos.
Lo que hace el carbono importante es la habilidad de los átomos de carbono de unirse entre sí y formar largas cadenas. Esas cadenas de carbono son la base de las moléculas que forman todos los sistemas vivos sobre la Tierra.
Dos átomos de carbono pueden unirse ya sea intercambiando un electrón, en cuyo caso decimos que es un enlace simple, o intercambiando dos electrones, en cuyo caso decimos que es un enlace doble. Los átomos de carbono también pueden formar enlaces triples compartiendo seis electrones.

Evidentemente, el número de enlaces que cualquier otro átomo puede formar depende del número de electrones en la órbita más externa.
El aspecto más importante de la química orgánica es la estructura tridimensional de las moléculas, porque esto es lo que determina si las moléculas “encajan entre sí” en sentido geométrico normal, de modo que se puedan formar los enlaces entre los átomos relevantes.
Dos moléculas que pueden unirse entre sí tal vez no sean capaces de hacerlo si no están orientadas correctamente. Se puede pensar en los átomos como en análogos a estructuras complejas que tienen pequeños puntos de velcro en ellas. Si la alineación de las moléculas no es la correcta (si los puntos de velcro no se sitúan juntos), entonces las moléculas no se unirán.

Hay un código para ayudarnos a dibujar moléculas orgánicas, porque cuando el número de átomos en una molécula llega a ser veinte, treinta o más, podemos perdernos por completo en los detalles.
La anotación estándar utilizada por los químicos para dibujar moléculas es como sigue:
1. Un enlace es representado por una linea recta entre dos moléculas.
2. Si la molécula en cuestión es de carbono, esto no se muestra específicamente en el dibujo.
3. Las moléculas de hidrógeno no se muestran en absoluto.
En este tipo de notación, lo que sería un dibujo complejo se convierte en algo muy simple.
Este es el ejemplo con una molécula de glucosa, uno de los azúcares básicos. En la parte de la izquierda la tenemos con todos los átomos presentes, y en el dibujo de la derecha está dibujada con las reglas que se han expuesto anteriormente.
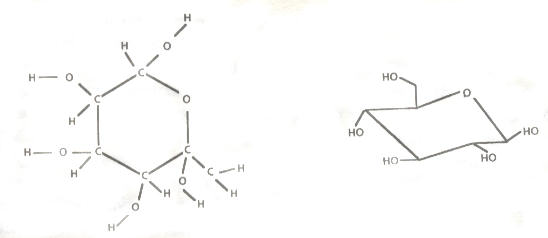
Dos formas de representar la molécula de glucosa




Nooooooooooooooooooooo noooooooooooo por qué?
Hasta en vacaciones tengo que ver quimica en blogs (estudio farmacia) tioooo esto ha sido a posta verdad? vale vale ¬¬ jajaja
Me encanta la quimica organica! :D